Deutérium
Fogalma
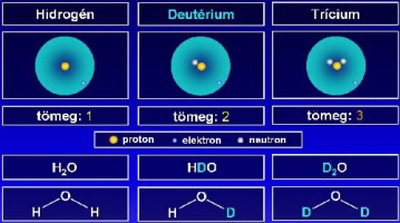
A deutérium vagy nehézhidrogén a hidrogén egyik stabil izotópja, melynek természetes előfordulása 1 atom 6500 hidrogénatomonként. A deutérium atommagját deuteronnak nevezik, egy protont és egy neutront tartalmaz, míg a normál hidrogén csupán egy protont.
A 2H kémiai jel azonosítja a deutériumot. A D nem hivatalos jelölést is gyakran alkalmazzák, holott a deutérium nem önálló kémiai elem. Természetes formájában deutériumgázként fordul elő: 2H2 vagy D2. Amikor normál hidrogénatomhoz (1H) kapcsolódik, akkor a gázt hidrogén deuteridnek hívják (legalábbis angol nyelvterületen).
Fizikai tulajdonsága
Fizikai tulajdonságai nem sokban térnek el a közönséges hidrogénétől; színtelen, szagtalan, íztelen gáz, moláris tömege kettővel több, 4 g/mol (az atommaghoz kapcsolódott neutron miatt).
Hármaspontja 18,73 K, 17 100 Pa.[1]
A deutérium -254,6 °C-on olvad és -249,7 °C-on forr.
Kémiai tulajdonságai
A deutérium kémiai szempontból a közönséges hidrogénhez hasonlóan viselkedik, bár a nagyobb tömege miatt a deutériumot tartalmazó reakciók valamivel kisebb sebességgel mennek végbe, mint a megfelelő közönséges hidrogént tartalmazó reakciók. A két izotópot fizikailag tömegspektrométerrel lehet megkülönböztetni. Ezenfelül a deutériumvegyületek fizikai tulajdonságai eltérhetnek a hidrogénes megfelelőjüktől; például a D2O sokkal viszkózusabb mint a H2O. Mivel a deuteronnak a spinje +1, ezért bozon.
A deutérium helyettesítheti a normál hidrogént a vízmolekulában nehézvizet (D2O) képezve. Jóllehet nem szigorúan mérgező, a nehézvíz fogyasztása ártalmas lehet az egészségre.
Csillagászati jelentősége
A deutérium jelenléte a csillagokban fontos adat a kozmológia számára. Mivel a deutérium elbomlik a csillagban végbemenő fúzió során, nem ismerünk más folyamatot, mint az ősrobbanás nukleoszintézisét a deutérium előállítására. Így ez egy fontos érv az ősrobbanás mellett a világegyetem állandó állapotú elméletével szemben
A deutérium mentes víz és a rák
A deutérium felhasználása
- A világ vezető deutériumtermelője Kanada
- Ezt nehézvíz formájában neutronmoderátornak használja fel a CANDU-reaktorokban
- A neutronelnyelő képessége (abszorpció) sokkal kisebb, mint a közönséges hidrogéné, és ez teszi kiváló neutronmoderátor anyaggá.
- Ugyanezen okból használják hidrogéntartalmú anyagokban izotóphelyettesítésre (deuterizált minta), mert az így preparált anyagok sokkal alkalmasabbak a neutronszórásos vizsgálatokra az eredetiknél.
- A fúziós energiatermelés egyik ígéretes nyersanyaga.
Vegyületek
| Nehézvíz | D2O |
| Nehézammónia | ND3 |
| Nehézmetán | CD4 |


